Les chercheurs de Vector ont développé CRISPNAM-FG, un modèle d’IA fiable qui prédit le risque de complications du pied liées au diabète chez les patients sortis de l’hôpital tout en offrant une transparence totale dans la manière dont chaque décision est prise – répondant au besoin crucial d’IA interprétable en soins de santé, où comprendre le raisonnement des modèles est primordial pour l’adoption clinique. Cette percée démontre que les systèmes d’IA peuvent atteindre une grande précision tout en maintenant une interprétation complète, résolvant un défi fondamental qui a limité le déploiement de l’IA dans des milieux médicaux à enjeux élevés. Accédez à l’article complet ici.
TLDR : Découvrez des recherches révolutionnaires en IA en 3 minutes
Ce résumé concis fait le pont entre les avancées scientifiques complexes et la compréhension quotidienne. Idéal pour les passionnés et les non-chercheurs, commencez à écouter dès maintenant.
L’analyse de survie est une approche statistique pour analyser les données temporellement à l’événement et consiste essentiellement à étudier le temps nécessaire avant qu’un événement se produise (comme l’apparition de la maladie, la guérison ou la mort) et quels facteurs influencent ce moment. L’analyse traditionnelle de la survie vise à prédire le risque d’un seul événement, mais de nombreux scénarios réels impliquent plusieurs événements « concurrents » où en vivre un empêche d’autres de se produire. Pour les personnes diabétiques, cela peut inclure le risque de complications du pied en concurrence avec le risque de mortalité d’autres causes.
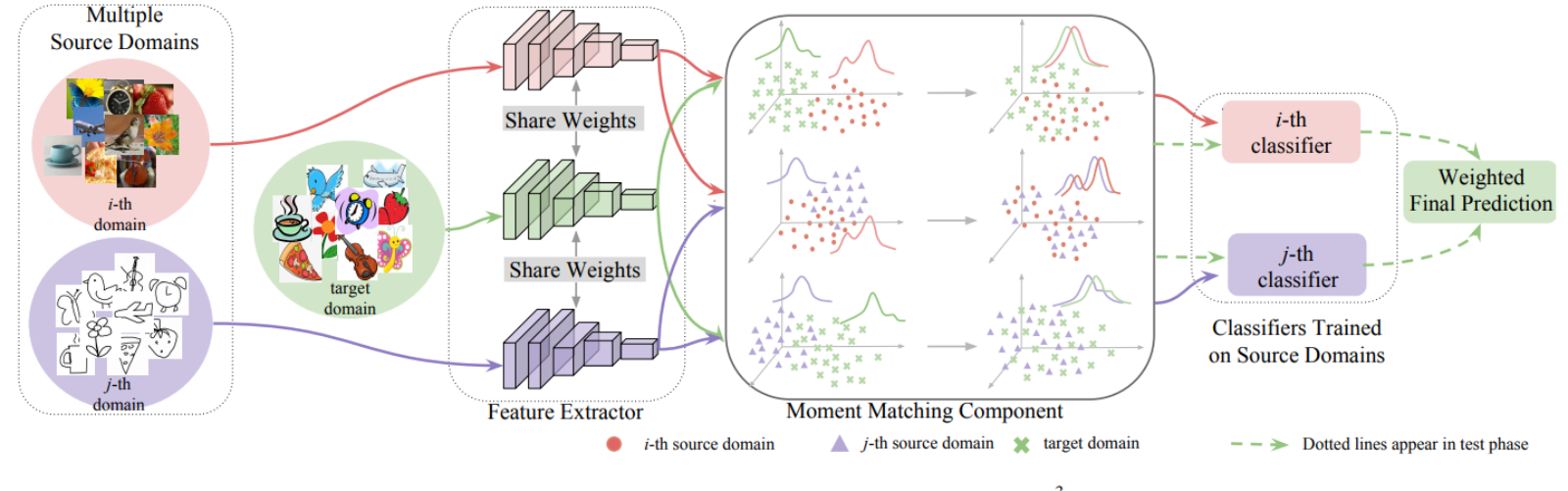
Des avancées récentes en apprentissage profond comme DeepHit et DeepSurv ont amélioré la performance prédictive pour des scénarios de risques concurrents, mais ces gains se font au détriment de l’interprétabilité, créant des modèles en boîte noire difficiles à faire confiance et à valider en pratique pour les cliniciens.
L’objectif de recherche de notre équipe est de permettre une prédiction précise et transparente des résultats temporels lorsque plusieurs risques coexistent, tout en maintenant un niveau d’interprétabilité qui soutient la confiance clinique, la validation et la prise de décisions politiques. Ce travail démontre que des performances prédictives élevées et une interprétabilité intrinsèque peuvent coexister dans des risques concurrents, l’analyse de survie pour une application réelle en soins de santé.
Ce travail représente un effort collaboratif entre Vector Institute, GEMINI, Unity Health et Diabetes Action Canada, réunissant expertise méthodologique, données hospitalières à grande échelle et connaissances du domaine en soins du diabète. Ensemble, l’équipe de recherche a développé CRISPNAM-FG (Concurrenting Risks Survival Prediction using Neural Additive Models : Fine Gray), un modèle de survie intrinsèquement interprétable qui gère les risques concurrents en utilisant la formulation Fine-Gray tout en maintenant à la fois le pouvoir prédictif de l’apprentissage profond et l’interprétabilité des modèles statistiques classiques.
Le défi de l’interprétabilité dans l’analyse de la survie
L’interprétabilité du modèle est cruciale pour établir la sécurité de l’IA et la confiance des cliniciens dans les applications médicales. Les modèles récents d’apprentissage profond ont obtenu de très bonnes performances prédictives, mais leur transparence limitée en tant que modèles en boîte noire nuit à leur intégration dans la pratique clinique.
Les approches de survie profonde existantes pour les risques concurrents, y compris DeepHit et Neural Fine-Gray, manquent d’interprétabilité intrinsèque, particulièrement au niveau des fonctionnalités. Cette opacité rend difficile la compréhension des contributions individuelles des caractéristiques aux prédictions de risque entre différents événements concurrents.
Les méthodes d’explication post-hoc comme LIME et SHAP ont des limites. Ils souffrent généralement d’une faible fidélité, ce qui mène à des explications infidèles ou trompeuses, et peuvent être facilement trompés. Contrairement aux modèles de survie profonde en boîte noire, l’approche CRISPNAM-FG est intrinsèquement interprétable et ne repose pas sur des méthodes d’explication post-hoc, souvent instables et difficiles à valider dans les milieux de soins de santé.
Architecture CRISPNAM-FG : Construire l’interprétabilité à partir de zéro
La contribution clé est l’intégration du cadre des risques concurrents Fine-Gray avec les modèles additifs neuronaux dans une architecture unique, entraînable de bout en bout. Chaque variable clinique est modélisée indépendamment à l’aide d’un petit réseau de neurones, permettant au système de capturer des effets non linéaires tout en préservant la transparence au niveau des caractéristiques.
Fondation du modèle additif neuronal
En suivant le cadre du Modèle Additif Neural, chaque fonctionnalité d’entrée est traitée par son propre réseau neuronal dédié, appelé FeatureNet. Ces sous-réseaux spécifiques à chaque caractéristique apprennent la contribution non linéaire de chaque caractéristique individuelle au score global de risque tout en préservant l’interprétabilité en isolant les effets des caractéristiques.
Chaque FeatureNet reçoit une entrée scalaire et produit une représentation cachée à travers des réseaux neuronaux feedforward entièrement connectés avec des fonctions d’activation tangente hyperbolique.
Projections spécifiques au risque
Le modèle permet à chaque caractéristique du patient d’influencer différents résultats de différentes façons. Par exemple, un taux de sucre élevé dans le sang pourrait augmenter fortement le risque de complications au pied tout en ayant un effet différent sur le risque de mortalité. Cette flexibilité est cruciale car les mécanismes biologiques à l’origine de chaque résultat peuvent être distincts.
Pour chaque variable et chaque résultat concurrent, le modèle apprend des transformations distinctes qui capturent comment cette variable contribue au risque. Pour assurer des comparaisons équitables entre différents résultats, ces transformations sont standardisées à la même échelle. Cela empêche qu’un résultat semble artificiellement plus important simplement en raison de différences dans les unités de mesure ou à l’échelle mathématique.
Formulation gris fin
L’approche Fine-Gray modélise la probabilité de vivre un événement spécifique au fil du temps, en tenant compte de la présence d’événements concurrents. Contrairement aux méthodes traditionnelles qui excluent les patients une fois qu’ils ont vécu un événement, Fine-Gray continue de suivre les patients même après qu’ils aient participé à un événement concurrent. Cela offre une image plus réaliste du risque dans des contextes cliniques où plusieurs résultats peuvent survenir.
Le modèle calcule le risque en combinant un risque de référence qui évolue au fil du temps avec des facteurs spécifiques au patient. Il convertit ensuite cela en incidence cumulative : la probabilité qu’un patient vive l’événement d’intérêt à un moment donné.
Interprétabilité par fonctions de forme
La principale force du modèle réside dans son interprétabilité intégrée. Plutôt que de produire des prédictions sans explication, elle génère des « fonctions de forme » qui visualisent comment chaque caractéristique de patient influence le risque.
Pour chaque variable clinique (comme l’âge, la glycémie ou la pression artérielle), le modèle crée une courbe montrant comment différentes valeurs de cette variable influencent le risque, séparément pour chaque résultat possible. Par exemple, vous pourriez constater comment l’augmentation des niveaux d’HbA1c augmente progressivement le risque de complications au pied par rapport à la mortalité.
Le système offre deux caractéristiques clés d’interprétabilité :
- Les graphiques de fonction de forme montrent comment chaque variable influence le risque sur toute sa plage de valeurs.
- Classements d’importance des caractéristiques qui identifient quels facteurs influencent le plus fortement chaque résultat concurrent
Cette transparence permet aux cliniciens de comprendre non seulement qui est à haut risque, mais aussi pourquoi le modèle arrive à cette conclusion, rendant les prédictions exploitables et vérifiables par rapport aux connaissances cliniques.
Validation dans le monde réel : Complications du pied diabétique en Ontario
Le problème clinique et l’ensemble de données GEMINI
Les chercheurs ont appliqué CRISPNAM-FG pour prédire les futures complications du pied diabétique après la sortie de l’hôpital, en utilisant des données provenant de plus de 100 000 patients répartis dans 29 hôpitaux en Ontario. Les complications du pied sont considérées comme l’issue principale, la mort à l’hôpital étant modélisée comme un risque concurrent.
L’ensemble de données, obtenu auprès de GEMINI, comprenait tous les patients adultes diabétiques sortis à domicile entre avril 2016 et mars 2023. Une complication du pied était définie comme la première hospitalisation pour un ulcère du pied, une infection, une gangrène ou une amputation. Après avoir appliqué les critères d’exclusion, la cohorte finale comprenait 107 386 patients. Les caractéristiques des patientes comprenaient un âge médian de 72,0 ans, avec 46,2% de femmes. La cohorte présentait une charge de comorbidité significative, 39,8% ayant un indice de comorbiditéde Charlson de 1 sur 1, et 28,4% un indice de 2 ou plus.
Performance du modèle
CRISPNAM-FG a démontré une forte performance discriminatoire sur l’ensemble de données GEMINI, obtenant des résultats compétitifs comparativement aux modèles existants de risques de concurrence profonde. Nous avons évalué le modèle à l’aide de deux mesures standard. TD-AUC (aire dépendante du temps sous la courbe) mesure à quel point le modèle distingue les patients qui vont vivre un événement ou non à un moment donné, avec des valeurs plus proches de 1,0 indiquant une meilleure discrimination. TD-CI (indice de concordance dépendant du temps) évalue également si le modèle classe correctement les patients selon leur risque, des valeurs plus élevées indiquant un ordre de risque plus précis.
Pour les complications du pied (Risque 1), le modèle a atteint des valeurs TD-AUC de 0,766 ± 0,042 au 25e percentile, 0,763 ± 0,047 à la médiane, et 0,763 ± 0,052 au 75e percentile. Pour le risque concurrent de mortalité (Risque 2), les valeurs TD-AUC étaient de 0,739 ± 0,057, 0,726 ± 0,058, et 0,707 ± 0,060 pour les mêmes percentiles.
Le modèle a démontré une forte performance discriminatoire comparée aux modèles de risques en concurrence profonde existants, tout en produisant des schémas de risque cliniquement cohérents qui correspondent aux connaissances médicales.
Perspectives cliniques issues des fonctions de forme interprétables
Les fonctions de forme sont le mécanisme d’interprétabilité central dans CRISPNAM-FG. Ce sont des courbes apprises qui montrent comment chaque caractéristique individuelle influence la prédiction du modèle à travers sa plage de valeurs. Contrairement aux modèles linéaires traditionnels où chaque caractéristique a un seul coefficient, les fonctions de forme peuvent capturer des relations non linéaires. Par exemple, ils pourraient montrer que le risque augmente lentement à faibles niveaux de HbA1c, mais s’accélère rapidement à des valeurs plus élevées. Chaque caractéristique a sa propre fonction de forme, et la prédiction finale est simplement la somme de toutes ces contributions individuelles. Cette structure additive est ce qui rend CRISPNAM-FG interprétable : les cliniciens peuvent examiner chaque fonction de forme indépendamment pour comprendre exactement comment le modèle utilise chaque variable pour calculer le risque.
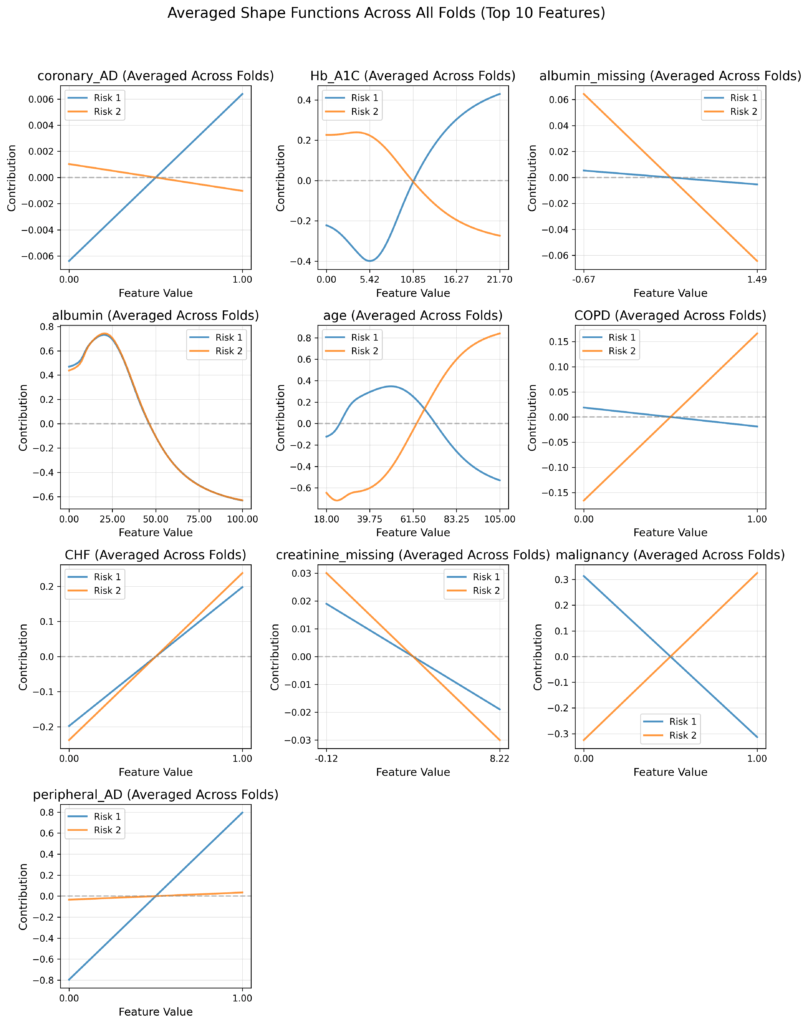
Les fonctions de forme calculées à partir du modèle CRISPNAM-FG entraîné sur l’ensemble de données GEMINI ont révélé des motifs cliniquement significatifs et parfois contre-intuitifs qui démontrent la capacité du modèle à capturer des relations cliniques complexes :
- Contrôle glycémique (HbA1c) : Les fonctions de forme montrent un schéma fascinant où des valeurs plus élevées d’HbA1c augmentent le risque de complications au pied comme prévu, mais diminuent en réalité le risque de mortalité. Cette découverte contre-intuitive démontre la capacité du modèle à révéler des relations cliniques complexes, en particulier celle des patients ayant un mauvais contrôle glycémique qui peuvent être plus susceptibles de développer des complications au pied avant de vivre des événements mortels.
- Comorbidités cardiovasculaires : La présence de maladie coronarienne montre une contribution accrue au risque de complications du pied, conformément aux connaissances médicales établies sur la relation entre les maladies cardiovasculaires et les complications diabétiques. L’insuffisance cardiaque congestive (ICC) démontre une contribution croissante tant aux complications du pied qu’à la mortalité, montrant comment les comorbidités cardiovasculaires influencent de multiples issues.
- Maladie vasculaire périphérique : Les fonctions de forme montrent une forte augmentation presque linéaire du risque de complications du pied avec la maladie artérielle périphérique, tout en ayant un impact minimal sur le risque de mortalité. Cela correspond parfaitement à la compréhension clinique selon laquelle la maladie vasculaire périphérique affecte directement la perfusion des membres et la cicatrisation des plaies.
- Schémas d’âge : L’âge présentait des schémas distincts pour les deux résultats. La contribution au risque de complications du pied augmente jusqu’à environ 60 ans avant de décliner, tandis que le risque de mortalité augmente de façon monotone avec l’âge. Cette divergence après 60 ans reflète probablement des risques concurrents, où les patients âgés succombent à des complications systémiques avant de développer des problèmes spécifiques au pied.
- État nutritionnel (albumine) : Des niveaux plus faibles d’albumine contribuent aux deux risques, mais la relation est plus prononcée avec le risque de mortalité, reflétant l’association connue entre l’hypoalbuminémie et de mauvais résultats. Les fonctions de forme montrent que l’effet protecteur de l’albumine diminue à mesure que les niveaux descendent sous les plages normales.
- Effets spécifiques à la maladie : Le modèle a correctement identifié que la maladie pulmonaire obstructive chronique (MPOC) ne contribue pas substantiellement au risque de complications du pied, mais augmente significativement le risque de mortalité. De même, la malignité montrait une association plus forte avec la mortalité qu’avec les complications du pied. Ces distinctions sont essentielles pour une planification appropriée après la sortie.
- Schémas de données manquants : Les valeurs manquantes pour la créatinine et l’albumine indiquaient un ordre sélectif de tests, où les cliniciens ne prescrivaient pas ces tests en l’absence de suspicion clinique de dysfonction rénale ou de complications liées à l’hypoalbuminémie.
Soutien aux soins préventifs et à l’allocation des ressources
CRISPNAM-FG est conçu spécifiquement pour soutenir les soins préventifs et l’allocation des ressources. En identifiant les patients à haut risque de complications au pied, les systèmes de santé peuvent prioriser le dépistage précoce, le suivi ambulatoire et les interventions multidisciplinaires reconnues pour réduire les amputations et les coûts en aval.
Parce que le modèle est interprétable, ses résultats peuvent être examinés, audités et communiqués aux cliniciens, aux patients et aux décideurs. Cette transparence permet aux professionnels de la santé de comprendre non seulement quels patients sont à risque, mais aussi pourquoi ils le sont et quels facteurs spécifiques influencent leur profil de risque élevé.
Cette interprétabilité est cruciale pour l’adoption clinique, car les cliniciens peuvent valider le raisonnement du modèle par rapport à leur expérience clinique et utiliser l’attribution détaillée des risques pour guider des interventions ciblées. Par exemple, un patient signalé principalement pour un mauvais contrôle glycémique bénéficierait d’interventions différentes de celui signalé pour une maladie vasculaire.
Avantages et limites du modèle
CRISPNAM-FG offre plusieurs avantages clés par rapport aux approches existantes :
- Interprétabilité intrinsèque : Contrairement aux modèles boîte noire, CRISPNAM-FG fournit un raisonnement transparent grâce à des fonctions de forme et des graphiques d’importance des caractéristiques qui montrent exactement comment chaque caractéristique contribue à chaque risque concurrent.
- Perspectives spécifiques au risque : Le modèle permet à la même variable d’avoir des effets différents sur différents résultats, révélant des relations cliniques complexes qui seraient obscurcies dans les modèles à résultat unique.
- Cohérence clinique : Les fonctions de forme produisent des schémas cliniquement significatifs qui s’alignent avec les connaissances médicales établies tout en révélant de nouvelles perspectives sur les interactions de risque.
- Transparence au niveau individuel : Le modèle permet de comprendre les contributions aux caractéristiques pour chaque patient, et non seulement l’importance globale des caractéristiques.
Nous reconnaissons que notre modèle ne capture pas les interactions au niveau des caractéristiques au-delà des effets additifs, ce qui peut limiter sa capacité à modéliser des relations complexes. De plus, bien que la performance en discrimination soit compétitive, la performance d’étalonnage du modèle est en retard par rapport à certaines alternatives comme DeepHit.
Voie d’implémentation réelle
Bien que CRISPNAM-FG ait été évalué à partir de données rétrospectives et n’ait pas encore été déployé en pratique clinique de routine, ce travail s’appuie sur le bilan éprouvé de l’équipe en matière de mise en œuvre clinique. Dans le cadre de la même initiative plus large, l’équipe de recherche avait déjà déployé un modèle de sous-distribution Fine-Gray antérieur à l’hôpital St Michael’s.
Cette expérience de mise en œuvre démontre la faisabilité pratique des modèles de survie interprétables dans des contextes cliniques réels et offre une voie pour étendre CRISPNAM-FG à des applications plus larges en soins de santé.
Conclusions et orientations futures
Les chercheurs démontrent qu’il est possible d’atteindre une performance prédictive compétitive dans une analyse de survie des risques concurrents sans sacrifier l’interprétabilité. CRISPNAM-FG propose une approche transparente et cliniquement alignée pour la prédiction des risques, bien adaptée au déploiement réel des soins de santé et à la prise de décision au niveau de la population.
Le modèle produit des scores de discrimination compétitifs tout en assurant la transparence grâce à des fonctions de forme qui révèlent des contributions détaillées à chaque risque. L’application aux complications du pied diabétique démontre l’utilité pratique du modèle dans des scénarios de soins de santé réels, révélant des perspectives cliniquement significatives sur les facteurs de risque et leurs impacts différentiels sur des résultats concurrents.
Les orientations de recherche futures incluent l’étude de réseaux de caractéristiques temporelles capables de capturer des contributions variables dans le temps pour chaque risque et le développement de fonctions de perte améliorées pour améliorer la performance d’étalonnage du modèle.
La proposition de valeur fondamentale pour les applications en santé est l’interprétabilité inhérente qui permet aux cliniciens de comprendre, valider et faire confiance aux prédictions des modèles, ce qui est une exigence cruciale pour une intégration sûre et efficace de l’IA en pratique clinique. Grâce à cet effort collaboratif entre Vector Institute, GEMINI et Diabetes Action Canada, l’équipe de recherche a démontré que l’avenir de l’IA en soins de santé ne réside pas dans le choix entre la précision et l’interprétabilité, mais dans l’architecture des deux systèmes unifiés et cliniquement précieux.

Créé par l’IA, édité par des humains, à propos de l’IA
Cet article de blogue fait partie de notre série « ANDERS – IA Développements notables expliqués & recherche simplifiée ». Ici, nous utilisons des agents d’IA pour créer des brouillons initiaux à partir de travaux de recherche, qui sont ensuite soigneusement édités et affinés par nos humains. L’objectif est de vous offrir des explications claires et concises des recherches de pointe menées par des chercheurs en Vector. Grâce à ANDERS, nous nous efforçons de combler le fossé entre les avancées scientifiques complexes et la compréhension quotidienne, en soulignant pourquoi ces développements sont importants et comment ils impactent notre monde.
Notes supplémentaires
1 L’Indice de comorbidité de Charlson est un système de notation qui quantifie le fardeau global de la maladie d’un patient en attribuant des points pour la présence de conditions chroniques spécifiques (comme le diabète, les maladies cardiaques ou le cancer), avec des scores plus élevés indiquant une comorbidité plus grave et un risque sanitaire accru.